
Каждый день в аптеки поступают сотни наименований товаров — от жизненно важных препаратов до косметики и БАД. Ошибка при приемке может стоить здоровья пациента: фальсифицированный препарат, нарушенная холодовая цепь, истекший срок годности — все это реальные риски, которые существуют на этапе до того, как товар попадет на полку.
Именно поэтому приемочный контроль в аптечных организациях — не формальность, а обязательная и строго регламентированная процедура. В этой статье разберем, кто ее осуществляет, на каких приказах она основана, как выстроить алгоритм приемки и избежать типичных нарушений.
Что такое приемочный контроль лекарственных средств
Приемочный контроль — это комплекс мероприятий по проверке товара, поступающего в аптечную организацию, на соответствие требованиям качества, безопасности и правильности оформления документов. Он охватывает весь аптечный ассортимент: медицинские изделия, БАД, косметику, пищевую продукцию.
Главная цель процедуры — не допустить реализацию фальсифицированных, недоброкачественных или контрафактных препаратов. В отличие от приемки товара в обычном магазине, где проверяется выборочная часть партии, аптечные организации обязаны проверять каждую единицу поступившей продукции. Это принципиальное отличие обусловлено тем, что речь идет о здоровье и жизни пациентов.
Помимо контроля качества, процедура решает еще несколько задач: подтверждает соответствие товара условиям договора с поставщиком, фиксирует количественные и качественные характеристики партии, обеспечивает прослеживаемость движения лекарственных препаратов в системе МДЛП.
Нормативная база приемочного контроля в аптеке
Процедура приемки строится на нескольких уровнях нормативных документов.
Основополагающим является Федеральный закон № 61-ФЗ «Об обращении лекарственных средств», который устанавливает общие требования к обороту лекарственных препаратов, в том числе к их приемке и хранению.
Ключевым отраслевым документом служит Приказ Минздрава России № 259н от 29 апреля 2025 года, который с 1 сентября 2025 года заменил утративший силу Приказ № 647н и стал действующим сводом правил надлежащей аптечной практики. Именно он регламентирует организацию зоны приемки, карантинной зоны, ведение журналов и стандартных операционных процедур (СОП).
Требования к условиям хранения и перевозки лекарственных средств закреплены в Приказе Минздрава России № 260н от 29 апреля 2025 года, который с 31 мая 2025 года заменил утратившие силу Приказы № 646н и № 706н. Этот документ устанавливает единые стандарты надлежащей практики хранения и перевозки лекарственных препаратов — от температурного режима до требований к зонированию складских помещений.
Для иммунобиологических препаратов действуют особые правила — требования к соблюдению холодовой цепи закреплены в СанПиН 3.3686-21 (Приложение 38).
Маркировка лекарственных средств кодами DataMatrix и работа с системой ГИС МДЛП (Мониторинг движения лекарственных препаратов) регулируются Постановлением Правительства № 1556 от 14.12.2018. Система МДЛП является частью платформы «Честный знак» (ГИС МТ).
Внутренний документ, на котором строится вся процедура в конкретной аптеке, — это СОП приемочного контроля, разработанный с учетом перечисленных требований.
Читайте также: Контроль качества на фармацевтическом предприятии: виды и методы
Кто осуществляет приемочный контроль в аптечной организации
Приемочный контроль в аптечных организациях осуществляет специально назначенная комиссия или уполномоченное должностное лицо. Состав комиссии и полномочия ее членов закрепляются приказом руководителя аптечной организации.
В состав комиссии включаются:
- Провизор или фармацевт, имеющий соответствующий допуск и знание ассортимента.
- Материально ответственное лицо, на которое возложена ответственность за сохранность товарно-материальных ценностей.
- При необходимости — заведующий аптекой или его заместитель.
Фармацевтические работники несут ответственность за профессиональную оценку качества товара: проверку маркировки, упаковки, соответствия препарата описанию, а также за сверку с сопроводительной документацией. Вспомогательный персонал (санитары, водители, грузчики) к непосредственной проверке не допускается — они могут участвовать только в физическом перемещении товара.
Важно: если в аптеке нет отдельной службы контроля качества, функции МОЛ и ответственного за приемку могут совмещаться у одного сотрудника, однако это должно быть четко прописано в его должностной инструкции и приказе руководителя.
Зона приемки и карантинная зона: требования к организации
Согласно правилам надлежащей аптечной практики, в каждой аптечной организации должна быть выделена специальная зона приемки. Ее назначение — обеспечить безопасное и корректное проведение всех процедур контроля до размещения товара на хранение.
К зоне приемки предъявляются следующие требования:
- Достаточная площадь для распаковки и осмотра поступившей продукции.
- Наличие рабочего стола, весового оборудования и сканера для считывания кодов DataMatrix.
- Соответствие температурного режима условиям хранения принимаемых товаров.
- Четкая визуальная разметка, отделяющая зону приемки от торгового зала и зон хранения.
Карантинная зона в аптеке — это отдельное, четко обозначенное место, куда помещается товар, не прошедший приемочный контроль или вызвавший сомнения. Она может располагаться как в зоне приемки, так и в другом помещении — при условии, что доступ к ней ограничен и она исключает смешение карантинного товара с готовым к реализации.
Основания для помещения товара в карантинную зону:
- Несоответствие документов или их отсутствие.
- Повреждение первичной или вторичной упаковки.
- Нарушение условий транспортировки (в том числе температурного режима).
- Подозрение на фальсификацию.
- Истечение или скорое истечение срока годности.
- Несоответствие маркировки требованиям законодательства.
Товар в карантине не может быть выдан покупателю или перемещен в торговый зал до завершения проверки и принятия решения — либо о принятии, либо о возврате поставщику или уничтожении.
Сопроводительные документы при поступлении товара в аптеку
Проверка сопроводительной документации — первый и обязательный этап любой приемки. Отсутствие или неправильное оформление хотя бы одного документа является основанием для отказа в приемке всей партии или ее части.
Базовый комплект сопроводительных документов включает: товарно-транспортную накладную (ТТН) или универсальный передаточный документ (УПД), счет-фактуру, декларацию соответствия или сертификат качества.
Перечень обязательных документов варьируется в зависимости от группы товаров.
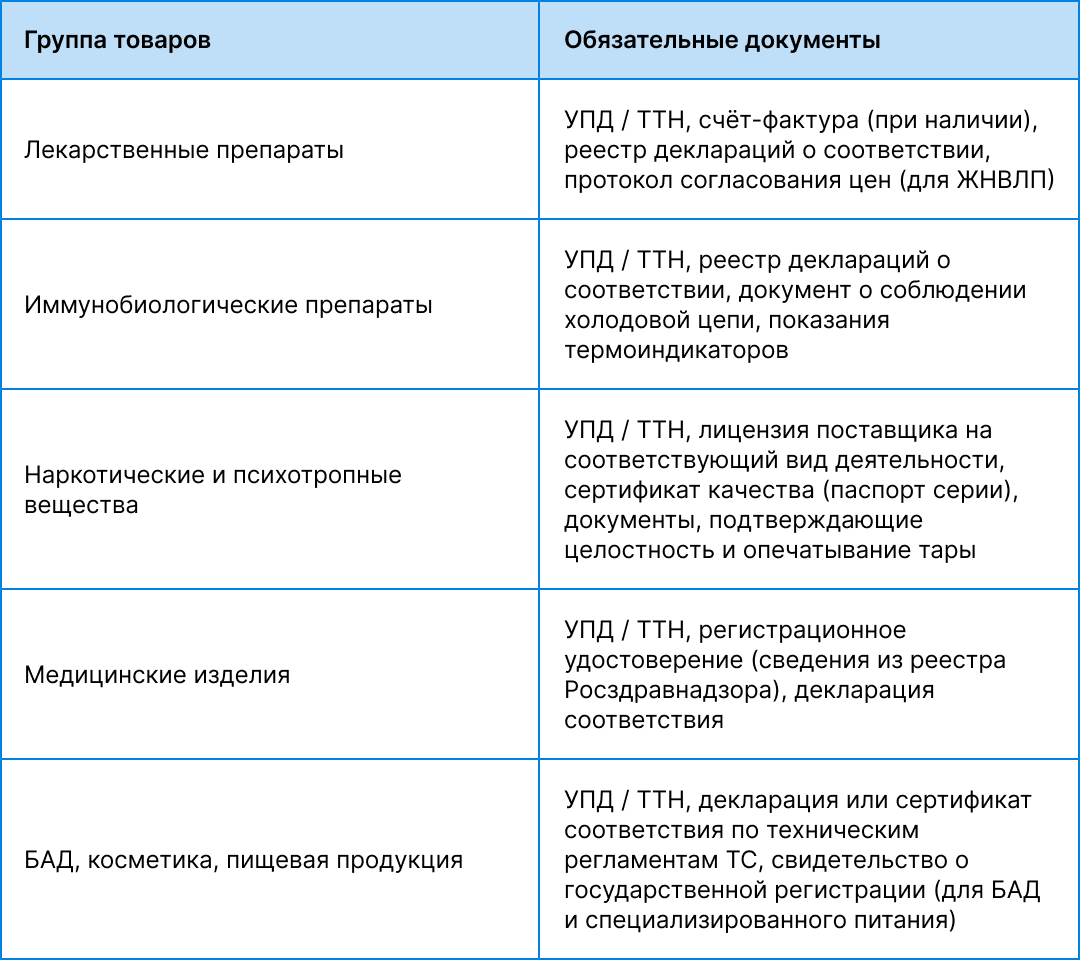
При проверке ТТН необходимо сверить наименование, количество и серии лекарственных препаратов с фактически поступившим товаром, убедиться в наличии подписей и печатей поставщика, проверить соответствие реквизитов организации-получателя. Декларации соответствия лекарственных средств проверяются по реестру Росздравнадзора — это позволяет исключить использование поддельных документов.
Алгоритм приемки товара в аптеке: пошаговая инструкция
Грамотно выстроенный алгоритм исключает ошибки и обеспечивает прослеживаемость каждой партии. Ниже приведена последовательность шагов, которая соответствует требованиям надлежащей аптечной практики.

Шаг 1. Встреча транспортного средства и предварительный осмотр. Уполномоченный сотрудник встречает водителя-экспедитора, проверяет наличие сопроводительных документов и осматривает транспортное средство: соблюдение температурного режима, целостность пломб и упаковки груза.
Шаг 2. Прием термолабильных и иммунобиологических препаратов. Иммунобиологические препараты принимаются в первую очередь. Фиксируются показания термоиндикаторов и терморегистраторов, данные вносятся в журнал регистрации соблюдения холодовой цепи. При выявлении нарушений температурного режима препараты помещаются в карантин.
Шаг 3. Проверка сопроводительной документации. Сверяются ТТН / УПД с фактическим количеством и наименованиями товара. Проверяются декларации соответствия, регистрационные удостоверения, протоколы согласования цен для ЖНВЛП.
Шаг 4. Количественная приемка. Проводится пересчет единиц по каждому наименованию. Выявленные расхождения фиксируются в акте расхождений при приемке.
Шаг 5. Качественная проверка. Осматриваются упаковки — первичная и вторичная. Проверяются маркировка, срок годности, серии лекарственных препаратов, целостность укупорки. При необходимости проверяются органолептические показатели (цвет, запах, консистенция).
Шаг 6. Сканирование DataMatrix-кодов. Каждая упаковка лекарственного препарата сканируется для подтверждения в системе ГИС МДЛП. Препараты с нечитаемым или отсутствующим кодом помещаются в карантинную зону до выяснения.
Шаг 7. Оформление документов. Подписываются ТТН / УПД, вносятся записи в журнал регистрации приемочного контроля, при выявлении расхождений составляется акт.
Шаг 8. Размещение товара. Товар, прошедший все этапы контроля, регистрируется в журнале приемочного контроля и передается на хранение в соответствующие зоны — с соблюдением условий хранения каждой группы.
Читайте также: Контроль качества в аптеке
Что проверяется при приемочном контроле лекарственных препаратов
Вы уверены, что в вашем медучреждении соблюдаются регламенты и стандарты?
Санитарные нарушения или ошибки в работе с пациентами грозят штрафами и предписаниями, а в худшем случае — приостановкой деятельности.
CheckOffice помогает удаленно контролировать любые операционные процессы в клинике и обеспечивает 100% достоверность проверок.
Проверка охватывает четыре основных показателя.
1. Описание. Внешний вид препарата должен соответствовать описанию в нормативной документации: цвет, форма, запах (при необходимости). Отклонения — основание для помещения в карантин и направления образцов в лабораторию.
2. Упаковка. Проверяется целостность первичной (блистер, флакон, ампула) и вторичной (картонная коробка) упаковки. Не допускаются вмятины, разрывы, следы вскрытия, нарушение укупорки.
3. Маркировка. На упаковке должны присутствовать: МНН и торговое наименование, дозировка, форма выпуска, серия, дата изготовления и срок годности, производитель, условия хранения, код DataMatrix. Маркировка лекарственных средств DataMatrix проверяется сканером с подтверждением в ГИС МДЛП.
4. Сопроводительные документы. Проверяется полный комплект документации. При поступлении лекарственных средств отдельно верифицируются декларации соответствия по реестру Росздравнадзора.
Если по итогам визуального осмотра возникают сомнения в качестве товара, образцы направляются в аккредитованную испытательную лабораторию. До получения заключения препараты хранятся в карантинной зоне и к реализации не допускаются.
Особенности приемки по группам товаров аптечного ассортимента
Иммунобиологические препараты. Это наиболее чувствительная группа с точки зрения условий хранения. Холодовая цепь при транспортировке должна быть непрерывной: температурный диапазон для большинства вакцин составляет от +2 до +8 °C. При приемке обязательно фиксируются показания термоиндикаторов, вложенных в каждую упаковку, и данные терморегистратора транспортного средства. Все результаты вносятся в отдельный журнал регистрации соблюдения холодовой цепи. Если температурный режим был нарушен, препарат не принимается — даже при наличии всех документов.
Наркотические и психотропные препараты. Приемка осуществляется строго по лицензии и в присутствии уполномоченных лиц. Тара должна поступать опечатанной; при приемке проверяется целостность пломб и сверяются номера печатей с указанными в сопроводительных документах. Вскрытие тары производится комиссионно с составлением акта. Любые расхождения немедленно фиксируются и передаются руководителю.
ЖНВЛП. Жизненно необходимые и важнейшие лекарственные препараты проходят стандартную приемку плюс обязательный контроль цен. Фактическая отпускная цена поставщика сверяется с протоколом согласования цен и предельными ценами, зарегистрированными в государственном реестре. Превышение зарегистрированной предельной цены является основанием для отказа в приемке.
Медицинские изделия. При приемке медицинских изделий проверяется наличие регистрационного удостоверения Росздравнадзора — без него изделие не может обращаться на российском рынке. Типичные нарушения: истекший срок действия регистрационного удостоверения, несоответствие наименования изделия в документах фактическому, отсутствие инструкции на русском языке.
Пищевая продукция, БАД, косметика. Для этих групп обязательны декларации или сертификаты соответствия техническим регламентам Таможенного союза (ТР ТС), а также свидетельства о государственной регистрации — для БАД и отдельных категорий косметики, перечисленных в Приложении 12 к ТР ТС 009/2011 (детская косметика, пилинги, средства для осветления и завивки волос и ряд других). Для остальной косметики СГР не требуется — достаточно декларации о соответствии.
Журнал регистрации приемочного контроля
Журнал регистрации приемочного контроля — обязательный внутренний документ аптечной организации, подтверждающий факт проведения проверки каждой поступившей партии. Он входит в систему качества аптеки и может быть запрошен при проверке Росздравнадзором.

Обязательные поля журнала:
- Дата поступления товара.
- Наименование поставщика.
- Наименование товара, лекарственная форма, дозировка.
- Серия и номер партии.
- Срок годности.
- Количество принятых единиц.
- Результат проверки (принят / помещен в карантин / возвращен).
- Подпись ответственного лица.
Журнал может вестись как в бумажной, так и в электронной форме — при условии обеспечения защиты от несанкционированного изменения записей. Каждая запись заверяется подписью сотрудника, осуществлявшего приемку. Исправления вносятся с указанием причины и подтверждаются подписью.
Срок хранения журнала нормативно не установлен и определяется локальным актом аптеки. На практике ориентируются на общий архивный минимум — не менее трех лет. Для журналов учёта наркотических и психотропных средств действуют специальные сроки в соответствии с Приказом Минздрава № 378н.
Читайте также: Аудит в аптечных сетях
Действия при выявлении несоответствий в ходе приемки
Несоответствия могут быть количественными (недостача, излишки), качественными (поврежденная упаковка, нарушение маркировки) и документарными (неполный комплект, ошибки в документах).
При выявлении любого несоответствия алгоритм действий следующий.
1. Фиксация. Несоответствие фиксируется в акте расхождений при приемке — документе, который составляется в двух экземплярах в присутствии представителя поставщика (или с его уведомлением). Акт подписывается комиссией.
2. Карантин. Спорный товар помещается в карантинную зону с соответствующей маркировкой («Карантин — не для продажи»).
3. Уведомление поставщика. Поставщику направляется претензия с приложением акта расхождений и фотоматериалов. Решается вопрос о возврате, замене или корректировке документов.
4. Работа с ГИС МДЛП. При выявлении проблем с DataMatrix-кодами (нечитаемый, дублирующийся, не найденный в реестре код) необходимо направить запрос через систему мониторинга движения лекарственных препаратов. Препарат не может быть принят в оборот до устранения расхождения.
5. Уведомление Росздравнадзора. Если есть основания полагать, что препарат является фальсифицированным или контрафактным, аптечная организация обязана уведомить территориальный орган Росздравнадзора. Самостоятельная реализация или уничтожение такого товара без разрешения контролирующего органа не допускается.
Читайте также: Внутренний контроль качества в медицинской организации: цифровизация и автоматизация
Типичные нарушения, выявляемые при проверках
По результатам плановых и внеплановых проверок Росздравнадзора чаще всего фиксируются следующие нарушения:
- Отсутствие утвержденного СОП приемочного контроля или его несоответствие фактическим процедурам.
- Нарушение порядка ведения журнала регистрации приемочного контроля — пропуски дат, отсутствие подписей, неполные записи.
- Отсутствие карантинной зоны или ее неправильная организация — смешение карантинного и готового к реализации товара.
- Приемка товара без полного комплекта сопроводительных документов.
- Нарушения при работе с ГИС МДЛП — несвоевременное подтверждение приемки, ошибки при сканировании кодов.
- Несоблюдение холодовой цепи при приемке иммунобиологических препаратов — отсутствие фиксации показаний термоиндикаторов.
- Приемка ЖНВЛП без проверки цен по протоколу согласования.
- Отсутствие приказа о назначении ответственного лица за проведение приемочного контроля.
Каждое из этих нарушений может повлечь административную ответственность по КоАП РФ, вплоть до приостановления деятельности аптечной организации.
Автоматизация приемочного контроля с помощью чек-листов
Даже при наличии грамотно разработанного СОП человеческий фактор остается главным источником ошибок: сотрудник забыл проверить термоиндикатор, не внес запись в журнал, пропустил сверку цен по ЖНВЛП. Цифровые чек-листы решают эту проблему системно.
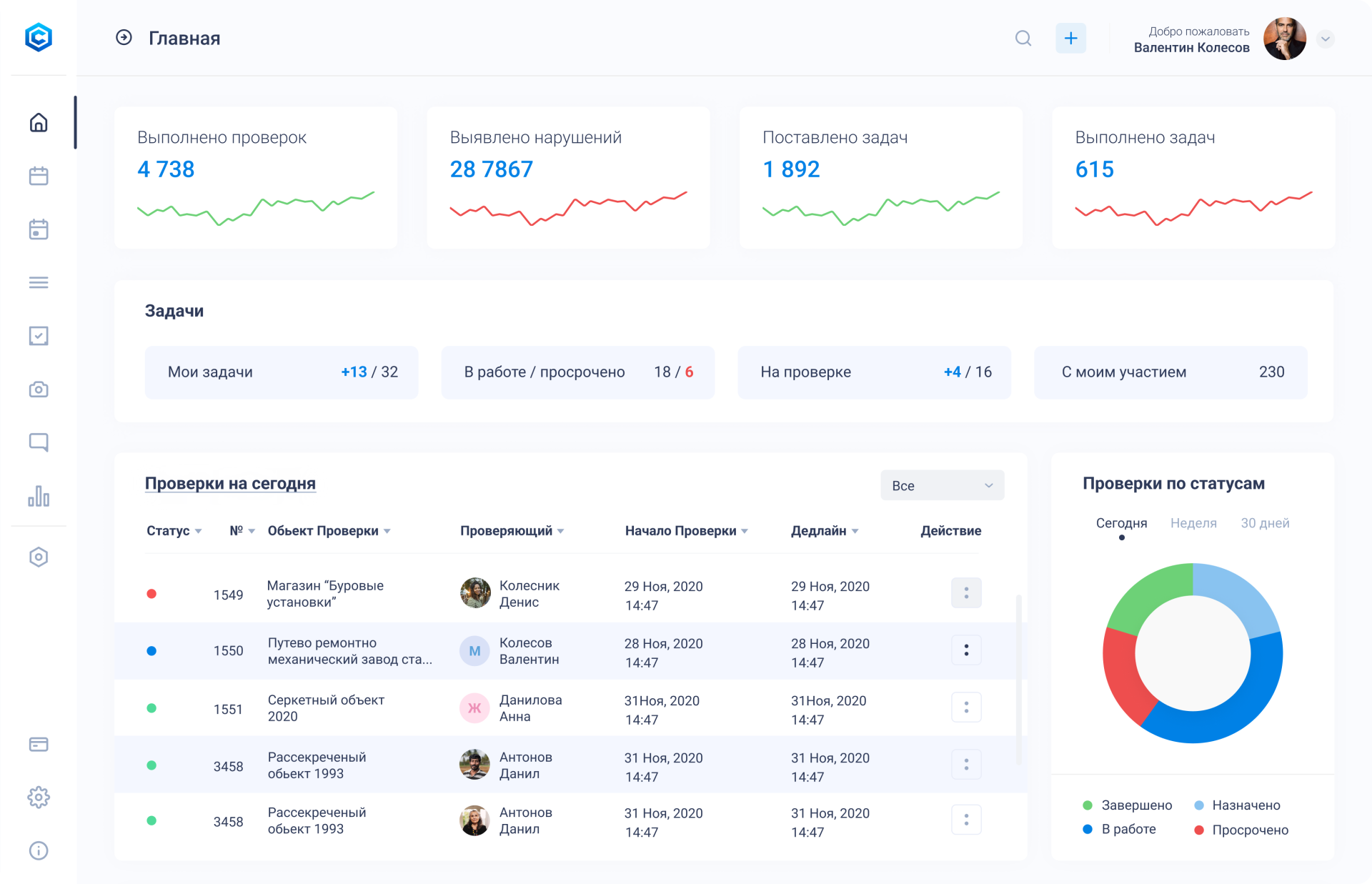
Чек-лист приемочного контроля, реализованный в специализированной платформе, позволяет:
- Стандартизировать последовательность шагов — сотрудник не может перейти к следующему пункту, не выполнив предыдущий.
- Автоматически фиксировать время и исполнителя каждого действия, формируя неизменяемый цифровой след.
- Мгновенно эскалировать выявленные несоответствия руководителю — без бумажных актов и телефонных звонков.
- Накапливать статистику по типичным нарушениям и выявлять системные проблемы в конкретных аптеках или сетях.
- Формировать готовые отчеты для внутреннего аудита и подготовки к проверкам Росздравнадзора.
Платформа CheckOffice предоставляет именно такой инструментарий для аптечных сетей. На ее основе можно создать цифровые чек-листы приемочного контроля под любую группу товаров аптечного ассортимента — от стандартных лекарственных препаратов до иммунобиологических и наркотических средств. Все данные хранятся централизованно, доступны в режиме реального времени и позволяют руководителю сети контролировать качество приемки в каждой точке — без визита на место.
Автоматизация не заменяет профессионализм фармацевтических работников, но снимает с них рутинную нагрузку и гарантирует, что ни один обязательный шаг не будет пропущен. В условиях роста требований регулятора и усложнения системы маркировки это становится не преимуществом, а необходимостью.































